
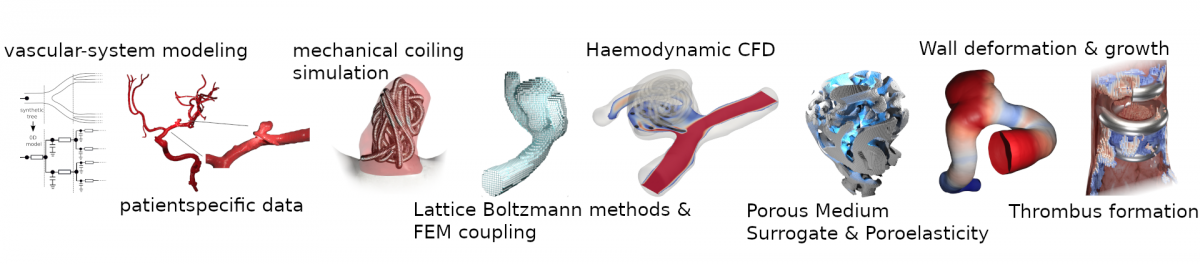
Medizinischer Hintergrund:
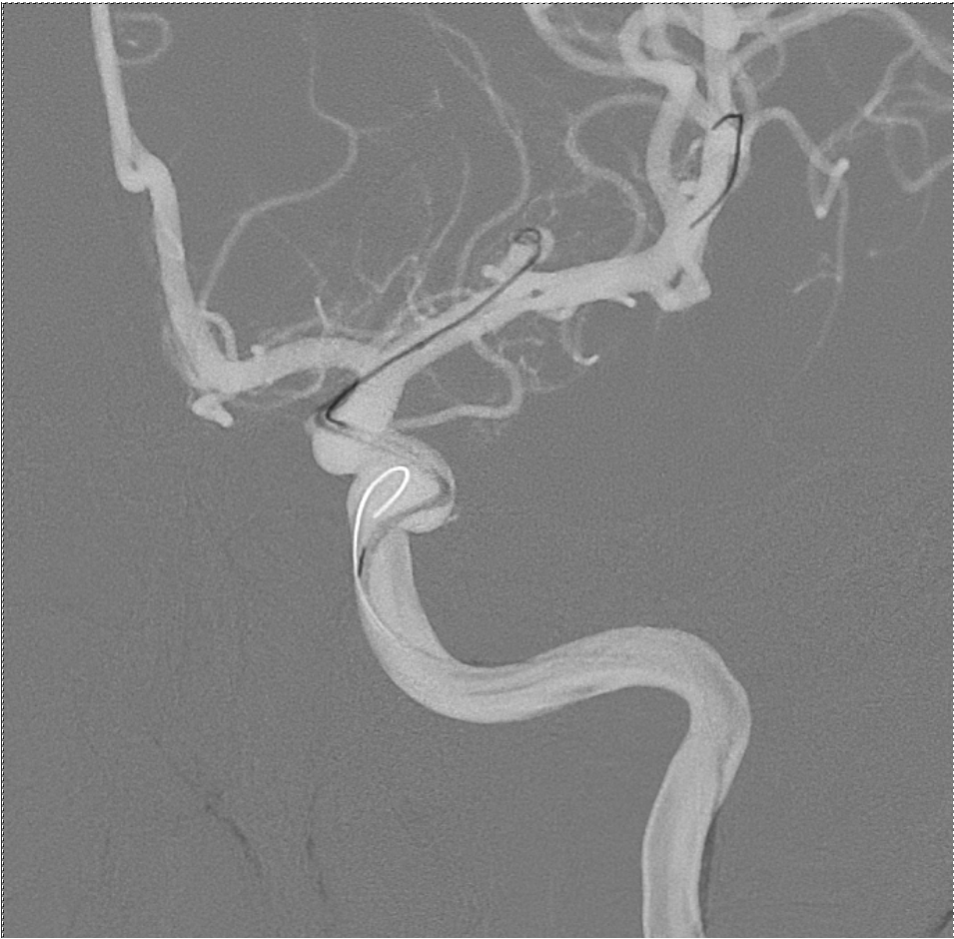
Begriffsklärung und Relevanz: Unter zerebralen Aneurysmen versteht man Aussackungen von Blutgefäßen im Gehirn, häufig verursacht durch Bluthochdruck oder Arteriosklerose, deren Wandstruktur einem erhöhten Ruptur-Risiko ausgesetzt ist. Reißt ein solches Aneurysma, so kann dies mit nahezu einer halben Million tödlicher Fälle jährlich drastische Folgen für den Patienten haben. Mit einer Prävalenz von etwa 3 % in der EU besteht damit eine hohe Dringlichkeit für die Weiterentwicklung diagnostischer sowie behandlungstechnischer Methoden.
Behandlung: Wird ein Aneurysma im Rahmen einer angiographischen, CT oder MRT Untersuchung festgestellt, muss abgewogen werden, ob, und wenn ja, wie behandelt werden soll. Dabei kommen insbesondere endovaskuläre Techniken wie das Coiling des Aneurysmas oder das Einsetzen von Flow-Divertern immer häufiger in Betracht.
– Coiling: Beim Coiling wird ein extrem weicher Mikrodraht über einen Katheter in das Aneurysma eingeführt, bis dieses volumetrisch möglichst gut ausgefüllt ist. Der dadurch im Aneurysma geformte Coil unterbindet oder verringert zumindest weiteren Blutfluss im kritischen Bereich, wobei die Bildung eines Thrombus um den Coil herum diesen Effekt noch weiter verstärkt.
– Flow-Diverter: Ein Flow-Diverter ist ein sehr engmaschiger Stent und wird in der Ader vor dem Aneurysma platziert. Dabei lenkt er, ebenfalls mit dem Ziel den Blutfluss im Aneurysma zu reduzieren, den Blutfluss daran vorbei, wobei die Position in der Ader durch ein Festdrücken an der Gefäßwand gehalten wird.
Risiken und Langzeitprognose: Bei der Auswahl des konkreten endovaskulären Devices, z.B. bereits bei der Auswahl eines geeigneten Coils spielen viele Parameter eine Rolle, von Länge, Dicke, Einführposition bis hin zu komplexen Mikrostrukturen im Coil-Material. Risiken sind z.B. dass Teile des Coils bei nicht-idealer Platzierung aus dem Aneurysma herausragen oder Teile des Aneurysmas nicht vollständig abgedeckt bzw. verschlossen werden. Solche Fälle werden im Rahmen der Raymond-Roy-Klassifikation kategorisiert. Folgen eines solchen unvollständigen Verschlusses können verbleibende Blutströme im Aneurysma mit einer pulsationsinduzierten weiteren Wand-Schwächung bis hin zum Nachwachsen des Aneurysmas aber auch die Bildung eines Ödems im Gewebe hinter dem Aneurysma sein. Aber auch im Falle eines vollständig okkludierten Aneurysmas kann es durch die Entzündungen der Aneurysma-Wand oder durch die komplexe Interaktion des Device-Materials mit dem sich bildenen Thrombus zu einem Schrumpfen des Coils (Coil-Compactification) mit ähnlichen Langzeitfolgen kommen.
Dies macht gerade auch die Analyse der Langzeitprognose von behandelten Aneurysmen neben der Optimierung der direkt Intervention zu einem essentiellen Forschungsaspekt.
Ziele:
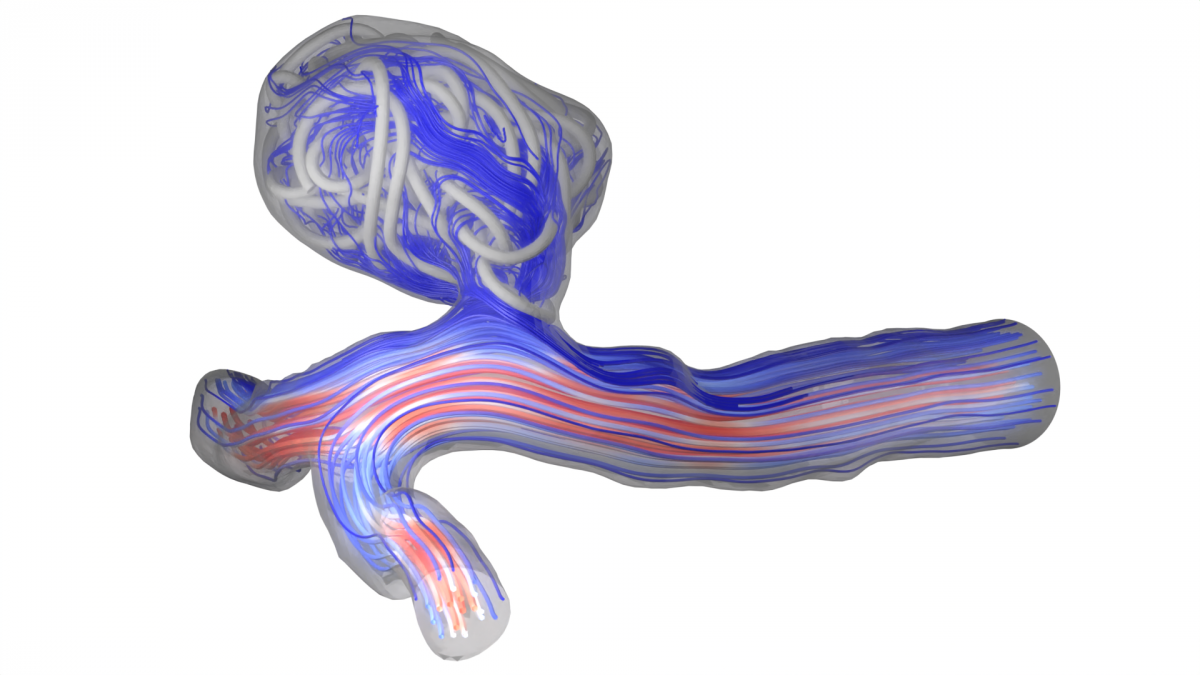
Wissenschaftliche Zielsetzung
Die Haupt-Zielsetzung dieses Projekts liegt in der Entwicklung von Methoden und Simulations-Werkzeugen, die den Verlauf einer endovaskularen zerebralen Aneurysma-Behandlung abbilden und Interventionalisten bei der Behandlungsplanung – von Diagnose, über Eingriffs-Optimierung bis zur Beurteilung der Langzeitperspektive – unterstützen.
Outreach & Networking: Neben dem rein wissenschaftlichen Aspekt ist auch die Kooperation innerhalb, aber auch die Netzwerkbildung über die Grenzen des SPPs hinaus ein zentrales Ziel, welches wir in der Hoffnung verfolgen Wissenschaftler und Ärzten mit klinischer/praktischer Erfahrung zusammenzubringen, um den aktiven Austausch zwischen diesen Gruppen zum Thema Behandlung zerebraler Aneurysmen in Deutschland zu stärken. Zu unseren dazu organisierten thematischen Workshops, siehe unten unter “Aktivitäten im Rahmen des SPPs”, sowie unter “Kollaborationen” zu unseren Networking und Kollaborations-Aktivitäten innerhalb des SPPs sowie international.
Lehre & Ausbildung: Mit der Vision eines praktisch anwendbaren Werkzeugs für Ärzte im klinischen Alltag findet unser Coil-Simulations-Tool bei Prof. Leonid Goubergrits (Charité Berlin) bereits Anwendung bei der Ausbildung von Studierenden, die daran virtuelle Coilings durchführen können und beurteilen lernen.
Methoden:
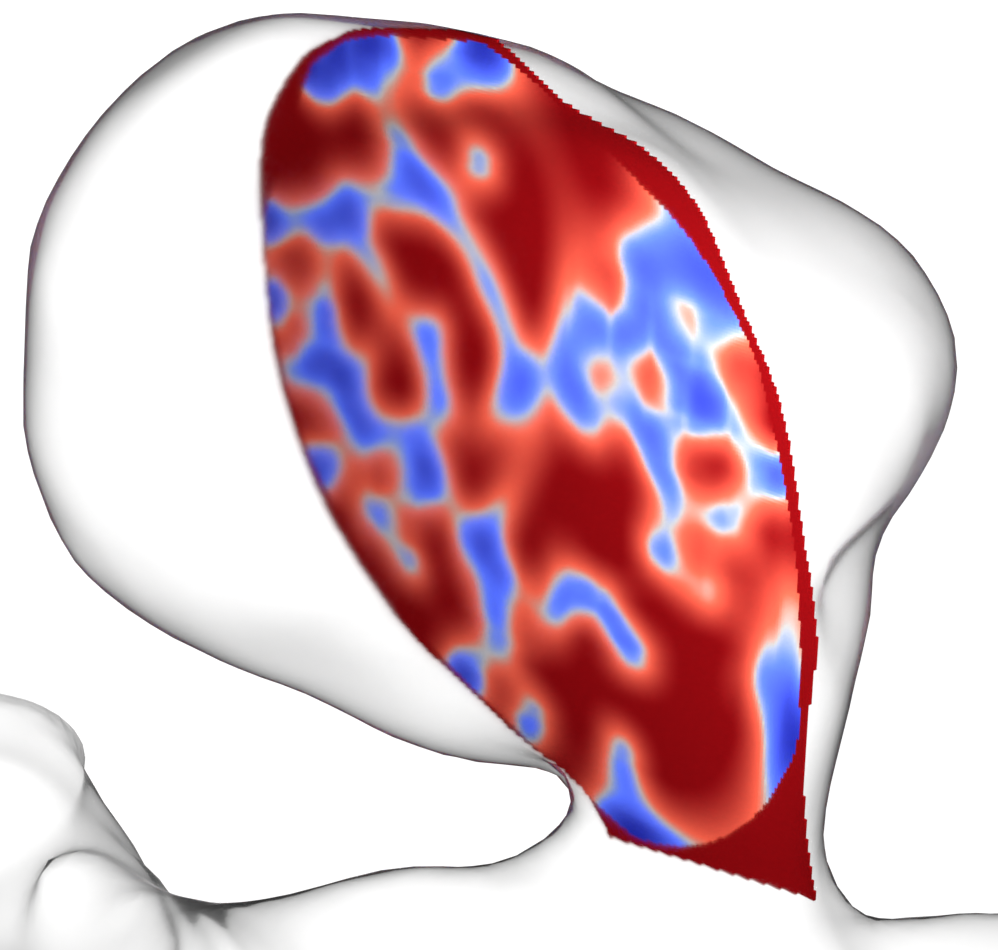
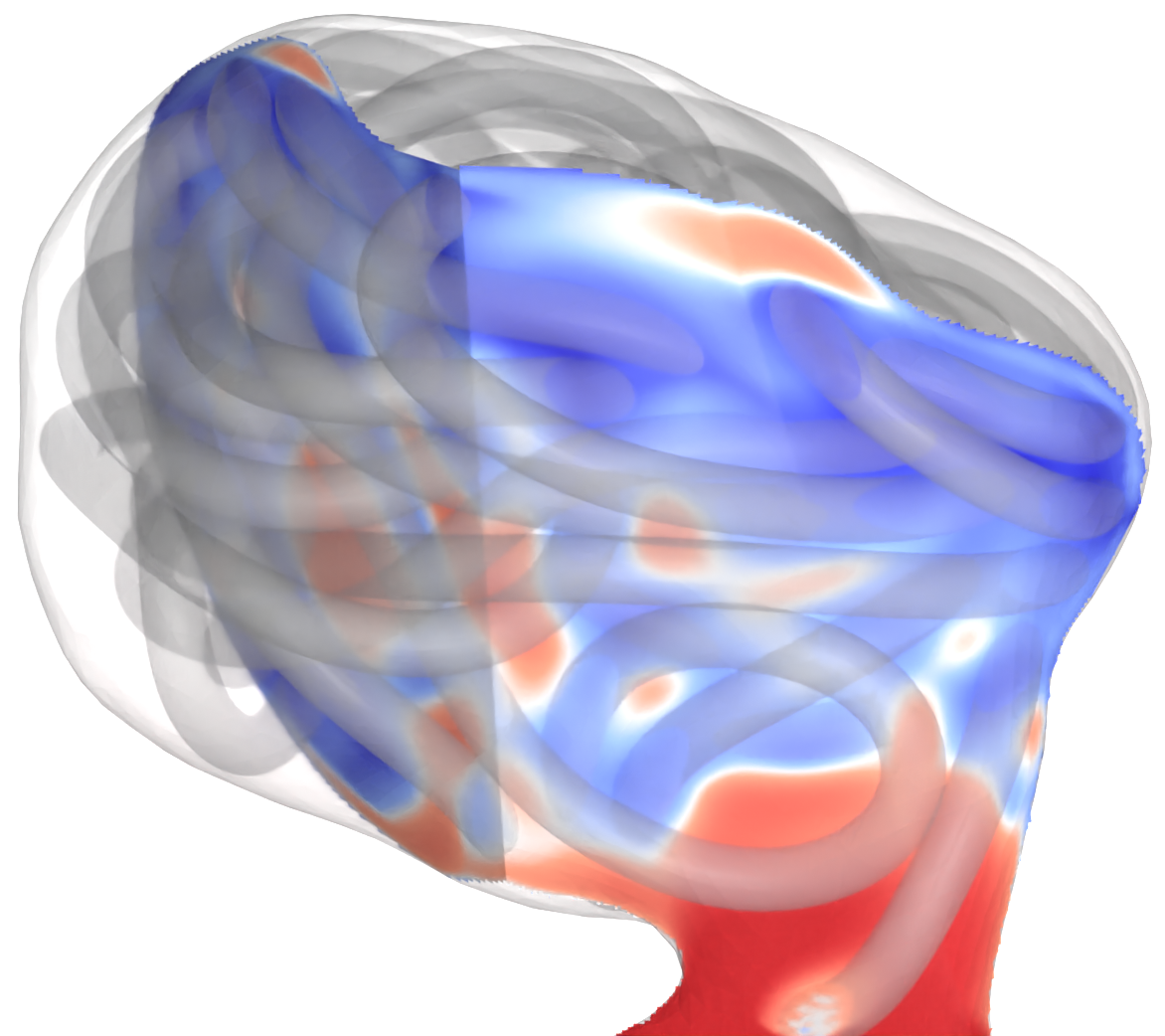

Durch entsprechende Mehrskalenmodelle wählt dieses Projekt optimale Behandlungstrategien für die endovaskuläre Intervention u.a. durch in-silico Testen verschiedener Devices oder Operationsansätze aus und sagt langfristige Behandlungsergebnisse voraus. Dafür werden poröse Medien Ansätze als Surrogate Modelle für endovaskuläre Devices und zur bio-aktiven Thrombus-Modellierung, gemischt-dimensionale Modelle zur Fluid-Struktur (Gefäßwand Pulsation), Struktur-Struktur (Device-Wand Interaktion) und Struktur-Solid (Gefäßwand-Gewebe) Kopplung verwendet. Hoch parallele Lattice-Boltzmann-Löser, gekoppelt mit Finiten-Elementen stellen die effiziente numerische Lösung der entstehenden Gleichungen auch in realistischen Szenarien sicher.
Phase I: In der ersten Phase des SPP-Projekts steht die direkte Eingriffsplanung im Vordergrund. Darunter fällt die realistische Simulation der Blutflussdynamik in patientenspezifischen Geometrien mit aneurysmapositionsabhängigen Randbedingungen und Auswertung relevanter Kenngrößen wie z.B. der Wandschubspannung zur Ruptur-Risiko Analyse. Ebenso ist die Modellierung von endovaskularen Devices inkl. der statistischen Berücksichtigung von Unsicherheiten ein entscheidender Aspekt, um bei der optimalen Wahl von Devices klinisch relevante Aussagen treffen zu können. Mit Hilfe von porösen Medien und poroelastischen Ansätzen kann der Einfluss von eingesetzten Devices auf die Bluflussdynamik und damit deren Okklusionsqualität modelliert und ausgewertet werden. Außerdem stellen sie eine Basis für die Modellierung und Simulation der Thrombusbildung dar, welche in der zweiten Projektphase ein weiterer Kern-Bestandteil sein wird. Mit der Lattice-Boltzmann zu Finite-Element Kopplung in Richtung Gefäßwand-Pulsation und -Dynamik und deren Umsetzung in entsprechenden High-Performance-Frameworks wird ebenfalls der Grundstein für entsprechend komplexere Modelle in Phase II gelegt.
Phase II: In Phase II liegt der Fokus auf der Langzeitperspektive des Patienten und der Rezidivvorhersage. Die in Phase I entwickelten in-silico Raymond-Roy-Okklusionsqualitätskriterien werden kalibriert und anhand experimenteller Daten unserer Kooperationspartner validiert. Im Bereich der endovaskularen Devices werden unsere komplexitätsreduzierten mechanischen Modelle um bioaktive Komponenten wie HydroCoils oder beschichtete Flowdiverter erweitert und neben dem Fluid auch Struktur-Struktur-Interaktionen mit der Gefäßwand einbezogen. Ausgehend von einem reduzierten Wandmodell werden biomechanische Modelle mit Entzündungsprozessen umgesetzt, die Materialeigenschaften der Wand verändern. Unsere Implementierung der gekoppelten Fluid-Struktur-Interaktion mittels Lattice-Boltzmann/Finiten Elementen wird auf einen Fluid-Struktur-Festkörper-Ansatz ausgeweitet, der das äußere Gewebe berücksichtigt, um den Ödembildungsprozess und den Thrombus im Inneren zu erfassen. Zur Quantifizierung und Vorhersage einer potenziellen Coilverdichtung wird ein phänomenologisches Kontraktionsmodell für den Thrombus entwickelt und mit der Wand- und Coilmechanik gekoppelt. Um die klinische Anwendbarkeit im Hinblick auf die Simulationsgeschwindigkeit zu verbessern und den Neurointerventionalisten einen praktischen Nutzen zu bieten, wird maschinelles Lernen als Prognosewerkzeuge eingesetzt.
Aktivitäten im Rahmen des SPPs:
Im Rahmen des SPPs organisieren wir Workshops mit thematischem Fokus auf dem Zusammenspiel von mathematischer Modellierung, numerischer Simulation und klinischer Anwendung und Praxis in Bezug auf die Behandlung zerebraler Aneurysmen. Teilnehmende sind typischerweise aus dem Bereich Mathematik/Informatik/Ingenieurswesen, genauso jedoch auch aus der Medizin um einen direkten Austausch von Theorie und Praxis und Erfahrungen zu schaffen. Wir laden sowohl andere SPP-Projektteams, wie auch externe Interessenten ein, bzgl. Teilnahme oder Co-Organisation mit uns in Kontakt zu treten.
- MFO Workshop: Multiscale Coupled Models for Complex Media: From Analysis to Simulation in Geophysics and Medicine
23 Jan – 29 Jan 2022 @Mathematische Forschungsinstitut Oberwolfach - Geplant: Workshop [zusammen mit Philipp Berg] zur Integration der SPP Themen in ein klinisches Anwendungswerkzeug
28 Jul – 31 Jul 2025 @Akademiezentrum Raitenhaslach
Involvierte Institutionen:
Kollaborationen:
Bereits über die Dauer der ersten Projektphase hinweg entstand ausgehend von dem SPP Projekt ein Netzwerk an (internationalen) Forschungskooperationen rund um die Behandlung und Simulation von Aneurysmen. Dabei liefern die im Rahmen des SPPs entstandenen Resultate Beiträge über die eigenen Projektgrenzen hinaus und finden so z.B. auch bei verwandten Behandlungsmethoden oder in der Ausbildung wissenschaftlichen und klinischen Nachwuchses Verwendung. Zu unseren engsten Kooperationen zählen dabei die Arbeiten mit:
- Universität Kapstadt: Zusammen mit Prof. Malebogo Ngoepe und Prof. Wei Hua Ho arbeiten wir an der Modellierung des Thrombus-Wachstums in Aneurysmen und insbes. auch deren experimenteller Validierung. Unser mechanisches Coiling Modell findet hier auch bereits Anwendung in der Forschung unserer Partner bei der Behandlung Arteriovenöser Malformationen.
- Charité Berlin: Zusammen mit Prof. Leonid Goubergrits (SPP Projekt mit PIs Goubergrits & Kühne) arbeiten wir neben der Integration und Etablierung des Coiling-Software-Tools im Lehrbetrieb auch an der weiteren Validierung des Modells bzgl. realistischer Coil-Formen sowie ebenfalls an Modellen zur Blut-Koagulation und deren experimenteller Bestätigung.
- TU Dresden: Zusammen mit Prof. Thomas Wallmersperger arbeiten wir an der experimentellen Charakterisierung des Quellverhaltens von beschichteten HydroCoils und der entsprechenden Modellierung im virtuellen Coiling-Modell. Solche HydroGel beschichteten Coils zeichnen sich u.a. durch eine nachträgliche Verdichtung der Aneruysma-Occlusion aus.
Antragsteller/innen:



Doktorand/innen:



Assoziierte Post-Docs



Publikationen:
2024
Numerical simulation of individual coil placement — A proof-of-concept study for the prediction of recurrence after aneurysm coiling Journal Article
In: [PrePrint], arXiv, 2024.
Finite elements for Matérn-type random fields: Uncertainty in computational mechanics and design optimization Journal Article
In: [PrePrint], arXiv, 2024.
A lattice Boltzmann method for non-Newtonian blood flow in coiled intracranial aneurysms Journal Article
In: [PrePrint], arXiv, 2024.
A Comprehensive Numerical Approach to Coil Placement in Cerebral Aneurysms: Mathematical Modeling and In Silico Occlusion Classification Journal Article
In: [PrePrint], arXiv, 2024.
Numerical simulation of endovascular treatment options for cerebral aneurysms Journal Article
In: [PrePrint], arXiv, 2024.
2023
Directional flow in perivascular networks: Mixed finite elements for reduced-dimensional models on graphs Journal Article
In: [PrePrint], arXiv, 2023.
Breaking Blood Flow with Wires in Aneurysm Coiling Treatment Simulations Online
SIAM, News (Ed.): 2023, visited: 19.12.2023.
2022
A 1D–0D–3D coupled model for simulating blood flow and transport processes in breast tissue Journal Article
In: International Journal for Numerical Methods in Biomedical Engineering, vol. 38, iss. 7, pp. e3612, 2022.
